HPV ARES - Unidade 2 - Vacinação contra HPV
Vacina papilomavírus humano 6, 11, 16 e 18 (recombinante)
Vacina papilomavírus humano 6, 11, 16 e 18 (recombinante)
A vacina HPV é apresentada na forma de suspensão injetável, unidose, acondicionada em embalagem contendo 10 frascos-ampola. Cada dose é de 0,5 ml.
Composição da vacina HPV
|
20 microgramas Proteína L12,3 do Papilomavírus Humano1 Tipo 6 40 microgramas Proteína L12,3 do Papilomavírus Humano1 Tipo 11 40 microgramas Proteína L12,3 do Papilomavírus Humano1 Tipo 16 20 microgramas Proteína L12,3 do Papilomavírus Humano1 Tipo 18 Excipientes: adjuvante sulfato de hidroxifosfato de alumínio amorfo (225 microgramas de Al), cloreto de sódio, L-histidina, polissorbato 80, borato de sódio e água para injetáveis (BRASIL, 2014). |
1Papilomavírus Humano = HPV.
2 Proteína L1 sob a forma de partículas tipo vírus produzidas em células de levedura (Saccharomyces cerevisiae CANADE 3C-5 (Estirpe 1895)) por meio de tecnologia DNA recombinante.
3 Adsorvida no adjuvante amorfo de sulfato de hidroxifosfato de alumínio (225 microgramas de Al).
Lembretes – vacina HPV
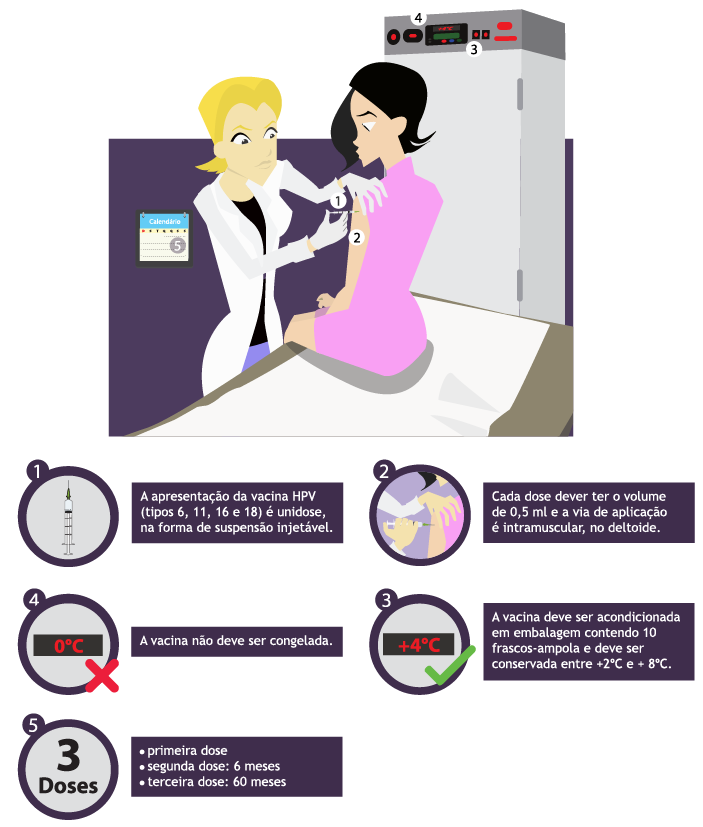
Fonte: (BRASIL, 2014).
Esquema de vacinação
O esquema vacinal inicialmente indicado e utilizado em vários países para a vacina HPV é de três doses, com esquema 0, 1-2 e 6 meses, e os intervalos mínimos entre as doses são (AMERICAN ACADEMY OF PEDIATRICS, 2012):
- intervalo entre a primeira e a segunda dose de um a dois meses (mínimo de um mês);
- intervalo mínimo entre a segunda e a terceira dose de quatro meses;
- intervalo mínimo entre a primeira e a terceira dose de seis meses.
No Brasil, o Ministério da Saúde adotará o esquema vacinal estendido, aplicando-se três doses aos 0, 6 e 60 meses, ou seja, o intervalo entre a primeira e a segunda dose é de 6 meses e a terceira dose é de 60 meses.Há estudos já publicados de imunogenicidade com duas doses (intervalo de seis meses) da vacina quadrivalente em comparação com três doses (0, 2 e 6), e os títulos de anticorpos não foram inferiores, havendo inclusive maiores títulos no primeiro grupo. A terceira dose após 5 anos da primeira é uma garantia adicional para a manutenção de uma resposta mais prolongada (KREIMER et al, 2011; DOBSON et al, 2013, NEUZIL et al, 2011).
Esta decisão foi tomada a partir da recomendação do Grupo Técnico Assessor de Imunizações da Organização Pan-Americana de Saúde (TAG/OPAS) (PAHO, 2013) e após aprovação pelo Comitê Técnico de Imunizações do Programa Nacional de Imunização (PNI), reconhecendo a necessidade de dados adicionais a longo prazo (BRASIL, 2014).
Até maio de 2013, a vacina HPV já havia sido introduzida em 51 países como estratégia de saúde pública (BRASIL, 2014).
|
Você sabia? |
|
Os resultados dos estudos de imunogenicidade com duas doses (intervalo de seis meses) da vacina quadrivalente no grupo de meninas de 9 a 13 anos, em comparação com três doses (0, 2 e 6) no grupo de mulheres jovens de 16 a 26 anos, não foram inferiores, havendo inclusive maiores títulos de anticorpos no primeiro grupo (DOBSON et al, 2013). Neuzil e colaboradores (2011) observaram que quanto maiores forem os intervalos entre as primeiras duas doses da vacina quadrivalente, maiores serão os títulos de anticorpos obtidos imediatamente antes da terceira dose, o que pode resultar em resposta imunológica mais robusta em adolescentes e adultos jovens. Kreimer e colaboradores (2011) observaram que, entre 802 mulheres na faixa etária entre 18 e 25 anos de idade que receberam duas doses (422 vacinadas e 380 controles), a eficácia foi de 84,1% (IC 95%, 50,2-96,3%). O esquema estendido já foi adotado por países como Canadá (Quebec e Colúmbia Britânica), México, Colômbia e Suíça. |
Esquemas alternativos da vacina HPV nas Américas
Fonte: (PAHO, 2014, adaptado).
|
Atenção! |
|
- O esquema vacinal será de 3 doses (0, 6 e 60 meses), ou seja, o intervalo entre a primeira e a segunda dose é de 6 meses; e entre a primeira e a terceira dose, de 60 meses; - Nas situações de atraso entre as doses, não haverá a necessidade de recomeçar o esquema vacinal; - Recomenda-se, para as adolescentes que tenham iniciado o esquema com a vacina bivalente, que terminem com a mesma vacina, nos próprios serviços onde iniciaram o esquema. No entanto, se não for possível, poderão completar o esquema vacinal com a vacina quadrivalente no serviço público; - Quando não é conhecida qual a vacina recebida e não há comprovação vacinal, a adolescente poderá iniciar o esquema com a vacina HPV quadrivalente disponível na rede pública; - Quando não é conhecido o número de doses já recebidas, iniciar o esquema com a vacina quadrivalente; - Não há dados disponíveis sobre a imunogenicidade ou eficácia das duas vacinas HPV quando usadas de forma intercambiável. Por isso, na medida do possível, aplicar a mesma vacina; - Se a adolescente já tem esquema completo da vacina bivalente, não revacinar com a quadrivalente. |
Para fazer download deste quadro, clique aqui.
População a ser vacinada
A população alvo da vacinação são as adolescentes do sexo feminino.
No ano da introdução da vacina (2014), serão vacinadas as adolescentes na faixa etária de 11 a 13 anos de idade; em 2015, as adolescentes com 9, 10 e 11 anos de idade; e partir de 2016, as adolescentes com nove anos de idade, conforme apresentado no quadro a seguir.
A população indígena é um grupo de maior vulnerabilidade às doenças. A população alvo da vacinação é composta por indígenas do sexo feminino na faixa etária de 9 a 13 anos no ano da introdução da vacina (2014) e de 9 anos de idade do segundo ano em diante (2015).
População alvo da vacina HPV
|
Ano |
População alvo |
|
|
|
|
|
Administração simultânea com outras vacinas
A vacina HPV pode ser administrada simultaneamente com outras vacinas do calendário de vacinação.
|
Atenção! |
|
Havendo possibilidade, aproveite o momento da vacinação contra o HPV e atualize o esquema vacinal para as vacinas dT (dupla tipo adulto), vacina hepatite B, SCR (sarampo, caxumba e rubéola) e febre amarela. |
Contraindicações
As contraindicações para a aplicação da vacina HPV são (AMERICAN ACADEMY OF PEDIATRICS, 2012):
- reação anafilática aos componentes da vacina;
- reação anafilática em dose anterior;
- aplicação em gestantes, uma vez que não há estudos conclusivos até o momento. Se a adolescente engravidar após o início do esquema vacinal, as doses subsequentes deverão ser adiadas até o período pós-parto. Caso a vacina seja administrada durante a gravidez, nenhuma intervenção adicional é necessária, somente o acompanhamento pré-natal adequado.
|
Você sabia? |
|
A vacina HPV é constituída de VLP, ou seja, apenas a “capa” do vírus. Essas estruturas (“capas” virais) são incapazes de replicação e são altamente imunogênicas , por isso essa vacina pode ser aplicada em pessoas imunodeprimidas (AMERICAN ACADEMY OF PEDIATRICS, 2012). |
Precauções
Abaixo algumas situações a serem observadas antes da vacinação:
Doença febril aguda grave
Na doença febril aguda grave, sobretudo para que os seus sinais e sintomas não sejam atribuídos ou confundidos com possíveis eventos das vacinas, recomenda-se o adiamento da vacinação. Adolescentes com resfriado poderão ser vacinadas.
Trombocitopenia
A vacina deve ser administrada com precaução em meninas com trombocitopenia (redução no número de plaquetas), ou qualquer outro distúrbio de coagulação, pelo risco de ocorrer sangramento ou hematoma após a injeção intramuscular.
Imunodeprimidas
A adolescente poderá ser vacinada.
|
Saiba mais... |
|
Nos estudos realizados com a vacina HPV, as mulheres que ficaram grávidas durante o recebimento do esquema vacinal tiveram a vacinação suspensa, e as doses que faltavam foram aplicadas após o nascimento da criança. Essas gestantes foram acompanhadas e não se observou aumento na taxa de abortos e malformações congênitas (CDC, 2010; DANA et al, 2009; AMERICAN ACADEMY OF PEDIATRICS 2012; CDC, 2007). Nos estudos realizados com a vacina HPV, foram acompanhadas mulheres que estavam amamentando e não se observou eventos adversos associados à vacina nos lactentes (CDC,2007; AMERICAN ACADEMY OF PEDIATRICS, 2012). |
Eventos adversos pós-vacinação (EAPV)
A vacina HPV é segura e bem tolerada, mas, como toda vacina, pode apresentar eventos adversos, conforme descritos no quadro a seguir.
Eventos adversos pós vacina HPV
| Tipo de evento adverso | Principais sinais e sintomas |
| Reações locais | ─ Dor, edema e eritema de intensidade moderada, no local de aplicação. |
| Manifestações sistêmicas | ─ Cefaleia;
─ Febre de 38ºC ou mais; ─ Síncope (ou desmaio). |
Fonte: (BRASIL, 2014 adaptado).
A síncope é uma alteração transitória da consciência acompanhada por perda da consciência e do tônus postural, causada pela diminuição do fluxo sanguíneo no cérebro, com recuperação espontânea, a maioria ocorre nos primeiros 15 minutos após a vacinação. É uma das causas mais comuns de perda parcial ou total da consciência e, embora seja um distúrbio benigno, com boa evolução, de modo geral, tem potencial para produzir lesões, como fraturas do quadril ou dos membros (SCHILLER; LOWY; MARKOWITZ, 2013).
|
Você sabia? |
|
Na Austrália e nos Estados Unidos, onde a vacina HPV já é aplicada, a taxa de síncope é baixa: 8,0/100.000 doses distribuídas (SLADE et al, 2009; CRAWFORD et al, 2011). Geralmente há um estímulo desencadeante, como dor intensa, expectativa de dor ou choque emocional súbito. Vários fatores, como jejum prolongado, medo da injeção, ambientes muito quentes ou superlotados, permanência de pé por longo tempo, podem aumentar a ocorrência de síncope (BRASIL, 2014). Portanto, para reduzir risco de quedas e permitir pronta intervenção caso ocorra a síncope, a adolescente deverá permanecer sentada e sob observação por aproximadamente 15 minutos após a administração da vacina HPV. |
|
Atenção! |
|
As adolescentes que apresentarem síncope poderão continuar o esquema vacinal. Na ocorrência de síncope, o caso deverá ser notificado em 24 horas por meio de ficha própria e seguir o fluxo já estabelecido pelo Sistema Nacional de Vigilância Epidemiológica de Eventos Adversos Pós-Vacinação (SIEAPV). Veja a figura a seguir. Fluxo de notificação de eventos adversos Fonte: (BRASIL, 2008). Apesar de a vacina HPV já ter sido amplamente estudada e ser utilizada de forma universal em diversos países, a investigação de EAPV é imprescindível para avaliar a segurança do produto. Para isso, tornam-se necessárias a notificação e a investigação de todos os eventos adversos graves (BRASIL, 2014). |
|
Atenção! |
|
A exemplo do que já é orientado para as outras vacinas, na ocorrência das situações descritas abaixo, com o objetivo de afastar qualquer associação com a vacina, a notificação também deverá ser realizada em 24 horas, seguindo o fluxo já estabelecido na figura anterior: - hospitalização por 24 horas; - disfunção ou incapacidade significativa e/ou persistente (sequela); - evento que resulte em anomalia congênita; - risco de morte; - óbito. Clique aqui para ter acesso ao "Manual de Vigilância Epidemiológica de Eventos Adversos Pós-Vacinação" (BRASIL, 2008). |